नमस्कार आज हम भौतिक विज्ञानं के महत्वपूर्ण अध्याय में से एक ऊष्मा (Heat) के विषय में अध्ययन करेंगे तथा साथ ही जानेंगे की ऊष्मा किसे कहते हैं?, गुप्त ऊष्मा क्या हैं? ऊष्मा की परिभाषा, ऊष्मा के प्रकार, ऊष्मा का सूत्र एवं मात्रक इत्यादि के विषय में खुल के अध्ययन करेंगे।
ऊष्मा किसे कहते हैं?
यह एक प्रकार की ऊर्जा ही है जो वस्तु के ठण्डे या गर्म होने के बारे में बताती है।
● किसी वस्तु का तापमान उसमें निहित आंतरिक ऊर्जा का परिणाम होता है। इस आंतरिक ऊर्जा को ‘ऊष्मा’ कहते हैं।
● यदि किसी वस्तु को ऊष्मा दी जाती है तो सामान्यत: इसके तापमान में वृद्धि होती है तथा वस्तु से ऊष्मा निकाल दी जाए तो इसके तापमान मे कमी आती है, केवल अवस्था परिवर्तन को छोड़कर। ऊष्मा का स्थानांतरण सदैव उच्च ताप वाली वस्तु से निम्न ताप वाली वस्तु की और होता है।
● वस्तु का गर्म या ठंडा होना ऊष्मा की मात्रा को बताता है। लेकिन वस्तु कितनी गर्म है या कितनी ठंडी है। यह केवल तापमान से ही पता चलता है।
● किसी वस्तु को स्पर्श करने पर यदि ऊष्मा उस वस्तु से त्वचा की ओर प्रवाहित हो तो वस्तु गर्म, जबकि त्वचा से वस्तु की ओर प्रवाहित होती वस्तु ठंडी हो जाती है।
● उदाहरण के लिए सर्दियों में लकड़ी और लोहे को छूने पर लोहा अधिक ठंडा प्रतीत होता है, क्योंकि लकड़ी की तुलना में लोहा ऊष्मा का अच्छा चालक है।
तापमान
- कोई वस्तु कितनी गर्म है अथवा कितनी ठण्डी है यह वस्तु के तापमान से ज्ञात होता है।
- ताप एक अदिश राशि है।
- इसकी विमा होती है।
- इसका मात्रक केल्विन, डिग्री सेल्सियस, फॉरेन्हाइट, रयूमर होता है।
● उपर्युक्त आधार पर कई पैमाने बनाए गए हैं। जिनमें प्रमुख सेल्सियस पैमाना, फॉरेनहाइट पैमाना, रोमर पैमाना एवं केल्विन पैमाना है।
1. डिग्री सेल्सियस पैमाना
● इस पैमाने पर जल का हिमांक 0°C तथा जल का क्वथनांक 100°C लिया जाता है।
2. केल्विन पैमाना
● इस पैमाने पर जल का हिमांक 273.15k तथा जल के क्वथनांक को 373.15 k लिया जाता है। इन दोनों के बीच की दूरी को 100 बराबर भागों में बाँट लेते हैं।
3. रोमर पैमाना
● इस पैमाने पर जल का हिमांक 0°R तथा जल का क्वथनांक 80°R है। उनके बीच के भाग को 80 बराबर भागों में बाँट देते हैं।
4. फॉरेनहाइट पैमाना
● इस पैमाने पर जल का हिमांक 32°F तथा क्वथनांक को 212°F लिया जाता है। इनके बीच के भाग को 180 बराबर भागों में बाँट देते है।
● सेल्सियस, केल्विन, फॉरेनहाइट और रोमर पैमानों के बीच परस्पर संबंध –
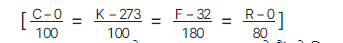
● (0K) तापमान को परम शून्य ताप कहते हैं जो कि प्रायौगिक रूप से संभव नहीं है।
● -40°C ऐसा तापक्रम है, जहाँ डिग्री सेंटीग्रेड और फॉरेनहाइट का मान एक ही होता है।
| पैमाना | इस पैमाने पर जल का हिमांक | इस पैमाने पर जल का क्वथनांक | अंतर |
| डिग्री सेल्सियस | 0oC | 100oC | 100 |
| केल्विन | 273.15 K | 373.15 K | 100 |
| फारेनहाइट | 32oF | 212oF | 180 |
| रियूमर | 0oR | 80oR | 80 |
| रेन्काईन | 491.67oRa | 671.62oRa | 180 |
ऊष्मा के कारक
ऊष्मा निम्न कारकों पर निर्भर करती है:-
1. द्रव्यमान:-
– किसी पदार्थ को दी गई ऊर्जा, पदार्थ के द्रव्यमान पर निर्भर करती है।
– यदि पदार्थ का द्रव्यमान अधिक होता है तो उसे अधिक ऊष्मा की आवश्यकता होती है।
– यदि पदार्थ का द्रव्यमान कम होता है तो उसे कम ऊष्मा की आवश्यकता होती है।
जैसे- 1 किग्रा. जल को गर्म करने के लिए दी गई ऊष्मा, 12 किग्रा. जल को दी गई ऊष्मा से अधिक होती है।
2. तापान्तर:-
– किसी पदार्थ के तापमान को बढ़ाना अथवा घटाना, ऊष्मा पर निर्भर करता है।
– यदि किसी पदार्थ का तापमान बढ़ाना है तो उसे अधिक ऊष्मा प्रदान करनी पड़ेगी तथा किसी पदार्थ का तापमान घटाना है तो उसे कम ऊष्मा देनी पड़ेगी।
3. पदार्थ की प्रकृति:-
– किसी पदार्थ को दी गई ऊष्मा, पदार्थ की प्रकृति पर निर्भर करती है। उदाहरण- जैसे m द्रव्यमान वाले जल को Q ऊष्मा देने पर उसके तापमान में वृद्धि कम होती है, इसी प्रकार m द्रव्यमान वाले दूध को Q ऊष्मा देने पर उसके तापमान में वृद्धि अधिक होगी।
– किसी पदार्थ को दी गई ऊष्मा ΔQ = m×s×d
यहाँ m पदार्थ का द्रव्यमान है।
d तापान्तर है।
s यहाँ विशिष्ट ऊष्मा है।
– 1 ग्राम जल का तापमान 1oC बढ़ाने के लिए दी गई ऊष्मा 1 कैलोरी ऊष्मा कहलाती है।
ऊष्मा का मात्रक:-
जूल, कैलोरी तथा अर्ग ऊष्मा के मात्रक होते हैं।
1 कैलोरी = 4.2 जूल
1 जूल = 14.2 कैलोरी
1 जूल = 107 अर्ग
1 BTU (ब्रिटिश थर्मल यूनिट) = 252 कैलोरी
विशिष्ट ऊष्मा (Specific Heat)

जल की विशिष्ट ऊष्मा
जल की विशिष्ट ऊष्मा सबसे अधिक होती है।
जल जितनी देर से गर्म होता है पुन: ठण्डा भी उतनी ही देर से होता है।
एक ग्राम जल को गर्म करने के लिए 1 कैलोरी ऊष्मा की आवश्यकता होती है उसी प्रकार एक लीटर जल को गर्म करने के लिए 1000 कैलोरी अथवा 4,200 जूल की आवश्यकता होती है।
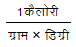
विशिष्ट ऊष्मा तापान्तर के व्युत्क्रमानुपाती होती है।
जल की विशिष्ट ऊष्मा के कारण ही इसका उपयोग रेडियेटर तथा रबर की गर्म पानी की बोतल में किया जाता है।
बर्फ की विशिष्ट ऊष्मा 0.5 कैलोरी/ग्राम × डिग्री सेन्टीग्रेड होती है।
वाष्प की विशिष्ट ऊष्मा 0.47 कैलोरी/ग्राम × डिग्री सेन्टीग्रेड होती है।
गुप्त ऊष्मा:-
जब पदार्थ की अवस्था परिवर्तन के समय पदार्थ तथा परिवेश के बीच एक निश्चित मात्रा में ऊष्मा स्थानांतरित होती है। इस ऊष्मा स्थानांतरण से पदार्थ का ताप परिवर्तित नहीं होता है और इसे अवस्था परिवर्तन में उपयोग कर लिया जाता है। ऊष्मा की इस निश्चित मात्रा को ही पदार्थ की ‘गुप्त ऊष्मा’ कहते हैं।
● एक निश्चित ताप पर पदार्थ की अवस्था परिवर्तन हेतु आवश्यक ऊष्मा ‘पदार्थ की गुप्त ऊष्मा’ कहलाती है।
● गुप्त ऊष्मा (L) = या
● गुप्त ऊष्मा का मात्रक = या
● इसकी विमा L2T-2 होती है।
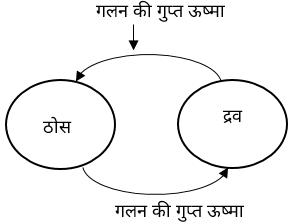
गलन की गुप्त ऊष्मा
0 डिग्री सेन्टीग्रेड की 1 ग्राम बर्फ की तुलना में 0 डिग्री सेन्टीग्रेड पर स्थित 1 ग्राम जल कम ठण्डा होता है क्योंकि जल में गलन की गुप्त ऊष्मा के रूप में 80 कैलोरी/ग्राम ऊर्जा अधिक होती है इसी अतिरिक्त ऊष्मा के कारण जल कम ठण्डा रहता है।
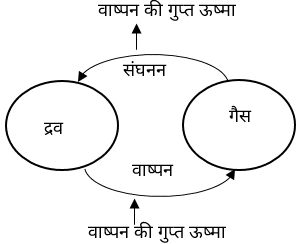
वाष्पन की गुप्त ऊष्मा
100 डिग्री सेन्टीग्रेड के जल की तुलना में 100 डिग्री सेन्टीग्रेड की वाष्प से जलना ज्यादा हानिकारक होता है क्योंकि वाष्प में गुप्त ऊष्मा के रूप में 536 कैलोरी/ग्राम ऊर्जा ज्यादा पाई जाती है।
● बर्फ के गलन की गुप्त ऊष्मा 80 कैलोरी/ग्राम होती है।
● जल के वाष्पन की गुप्त ऊष्मा 540 कैलोरी/ग्राम होती है।
● उदाहरण-
0 डिग्री सेन्टीग्रेड पर की 1 ग्राम बर्फ की तुलना में 0 डिग्री सेन्टीग्रेड पर स्थित 1 ग्राम जल कम ठण्डा होता है क्योंकि जल में गलन की गुप्त ऊष्मा के रूप में 80 कैलोरी/ग्राम ऊर्जा अधिक रहती है।
● 1 ग्राम पानी को वाष्प में बदलना हो तो 540 कैलोरी ऊष्मा देनी होगी।
● 1 ग्राम वाष्प से द्रव में बदलने पर 540 कैलोरी ऊष्मा मुक्त होती होगी।
● 1 ग्राम द्रव को बर्फ में बदलने पर 80 कैलोरी ऊष्मा मुक्त होगी।
● भाप उबलते जल की अपेक्षा अधिक ऊष्मा धारण करती है। इस कारण भाप से जलने पर अधिक कष्ट होता है।
गुप्त ऊष्मा:-

– इसकी विमा L2T-2 होती है।
ऊष्मीय प्रसार
जब किसी पदार्थ को ऊष्मा दी जाती है तो पदार्थ के परमाणु ऊष्मा अवशोषित कर कम्पन्न करने लगते हैं, जिससे दो परमाणुओं के बीच की अंतर-परमाण्विक दूरी बढ़ने लगती है, जिससे पदार्थ के आयतन में भी वृद्धि होती है इसे ही ऊष्मीय प्रसार (Thermal Expansion) कहते हैं।
उदाहरण-
– रेल की पटरियाँ बिछाते समय उनके बीच कुछ जगह रखी जाती है।
– बिजली के पोल पर तार बाँधते समय उन्हें कुछ ढीला रखा जाता है।
– काँच के पात्र में अत्यधिक गर्म द्रव को डालने पर काँच टूट जाता है।
– ठोसों में रेखीय प्रसार (Linear Expansion), क्षेत्रीय प्रसार (Area Expansion) तथा आयतन प्रसार (Volume Expansion) तीनों देखे जाते हैं जबकि द्रवों व गैसों में केवल आयतन प्रसार होता है।
ठोसों में ऊष्मीय प्रसार:-
1. रेखीय प्रसार:-


रेखीय प्रसार गुणांक:-
– 1 मीटर लंबे तार का तापमान 1 डिग्री सेन्टीग्रेड बढ़ाने पर तार की लम्बाई में होने वाला परिवर्तन तार का रेखीय प्रसार गुणांक कहलाता है।
– इसका मात्रक 10C या 1k होता है।
2. क्षेत्रीय प्रसार:-
– यह द्विवीमीय प्रसार है।
– इकाई क्षेत्रफल या 1 मीटर2 क्षेत्रफल वाली प्लेट का तापमान 1 डिग्री सेन्टीग्रेड बढ़ाने पर प्लेट के क्षेत्रफल में वृद्धि क्षेत्रीय प्रसार गुणांक के बराबर होती है।
– इसका मात्रक 10C या 1k होता है।
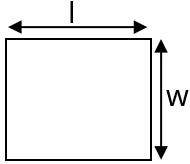
Ao = प्रारंभिक क्षेत्रफल
ΔT = ताप में परिवर्तन
AT = T ताप बढ़ाने पर क्षेत्रफल
3. आयतन प्रसार:-
– यह त्रिविमीय प्रसार होता है।
– इकाई आयतन की वस्तु का तापमान 1 डिग्री सेन्टीग्रेड बढ़ाने पर वस्तु के आयतन में हुई वृद्धि वस्तु का आयतन प्रसार गुणांक कहलाती है।
– इसका मात्रक 10C या 1k होता है।
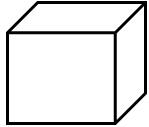

द्रवों में ऊष्मीय प्रसार:-
– द्रवों में केवल आयतन प्रसार होता है।
– किसी द्रव को पात्र में गर्म करने पर द्रव का स्तर पहले घटता है फिर बढ़ता है।
जल का गुण-
● सामान्यत: पदार्थो को गर्म करने पर उनका ऊष्मीय प्रसार होता है और ठंडा करने पर संकुचन लेकिन जल इसका अपवाद है।
● 0 डिग्री सेन्टीग्रेड से 4 डिग्री सेन्टीग्रेड के मध्य जल को गर्म करने पर आयतन में कमी आती है एवं घनत्व में वृद्धि होती है।
● 4 डिग्री सेन्टीग्रेड ताप के बाद जल सामान्य व्यवहार करता है जिसमें आयतन में वृद्धि एवं घनत्व मे कमी होती हो जाती है।
● जल का आयतन न्यूनतम 4ºc पर होता है।
● जल का घनत्व अधिकतम 4ºc पर होता है।
● बर्फ का आयतन जल से ज्यादा होता है।
● बर्फ का घनत्व जल से कम होता है।
● शुद्ध जल की बर्फ का घनत्व जल के घनत्व का 9/10वाँ भाग होता है।
● शुद्ध जल में बर्फ का 90%भाग पानी के अंदर और 10% भाग पानी के बाहर रहता है।
• अवस्था परिवर्तन- किसी ताप पर किसी पदार्थ का एक अवस्था से दूसरे में परिवर्तित होना ‘अवस्था परिवर्तन कहलाता है।
● ऊष्मा अवशोषित करके या उत्सर्जित करके पदार्थ की अवस्था में परिवर्तन किया जा सकता है।
● अवस्था परिवर्तन के समय पदार्थ के अणुओं के मध्य गतिज ऊर्जा नहीं बदलती, जबकि अणुओं की आंतरिक स्थितिज ऊर्जा में परिवर्तन होता है।
1. गलनांक एवं हिमांक/हिमन–
● जब पदार्थ की ठोस अवस्था द्रव अवस्था में बदलती है तो उसे गलन कहते है।
● जिस निश्चित तापमान पर गलन की क्रिया होती है, गलनांक बिन्दु कहलाता है।
● जब पदार्थ की द्रव अवस्था कुछ ऊष्मा उत्सर्जित कर ठोस अवस्था में परिवर्तित होती है इसे हिमन कहते हैं।
● जिस तापमान पर हिमन क्रिया होती है, उसे हिमांक बिन्दु कहते हैं।
● गलनांक और हिमांक एक ही ताप बिंदु होते हैं और इन पर ठोस एवं द्रव परस्पर तापीय साम्य पर होते हैं। जैसे- बर्फ का गलनांक बिन्दु 0 डिग्री सेन्टीग्रेड है।
● तापीय साम्य- ऊष्मा पारगम्य माध्यम से जुड़े निकायों के बीच ऊष्मा का प्रवाह न हो तो इसे ‘तापीय साम्य’ कहा जाता है।
● ऐसे ठोस पदार्थ जो द्रव में बदलने पर आयतन में प्रसार दर्शाते हैं उनका गलनांक दाब बढ़ाने पर बढ़ जाता है। उदाहरण- मोम।
2. क्वथनांक एंव संघनन बिंदु-
● वह निश्चित ताप जिस पर किसी पदार्थ की द्रव अवस्था गैस अवस्था में परिवर्तित होती है, ‘क्वथनांक’ कहलाता है।
● जब पदार्थ की गैसीय अवस्था द्रव अवस्था में परिवर्तित होती है, उसे संघनन कहते हैं तथा जिस तापमान पर गैस पुन: द्रव में बदलती है, उसे संघनन बिन्दु कहते हैं।
● बाह्म दाब बढ़ाने पर क्वथनांक बढ़ जाता है। उदाहरण- प्रेशर कुकर।
● पहाड़ी क्षेत्रों में वायुमंडलीय दबाव कम होने के कारण क्वथन कम ऊष्मा देने पर ही प्रारंभ हो जाता है, जिससे खाना पकाने में अपेक्षाकृत अधिक समय लगता है।
● पानी में नमक मिला दिया जाए तो पानी का क्वथनांक बढ़ जाता है।
3. वाष्पीकरण- सामान्य ताप पर भी किसी द्रव की खुली सतह से द्रव का गैस अवस्था में परिवर्तित होना वाष्पीकरण कहलाता हैं।
● कूलर की हवा वाष्पीकरण के कारण ठंडी होती है।
● शरीर से पसीना सूखने के दौरान वाष्पीकरण के लिए ऊष्मा त्वचा से प्राप्त की जाती है, जिस कारण शरीर को ठंडा करने में मदद मिलती है।
● गीले कपड़ों का सूखना
● आर्द्रता- वायु में आर्द्रता होने पर जल का वाष्पीकरण धीरे होता है। इसी कारण वर्षा ऋतु में कपड़े देर से सूखते हैं।
● तापमान- तापमान ज्यादा होने पर वाष्पीकरण तेज होता हे।
● दाब- अधिक दाब होने पर वाष्पीकरण की दर घट जाती है।
ऊष्मा संचरण:-
– माध्यम में या माध्यम की अनुपस्थिति में ऊष्मा का एक स्थान से दूसरे स्थान तक प्रवाह, ऊष्मा संचरण कहलाता है।
– यह तीन विधियों से होता है-
1. चालन
2. संवहन
3. विकिरण
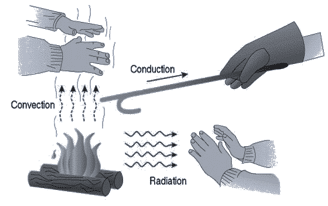
1. चालन- इस विधि में पदार्थ के कण गति किए बिना ही ऊष्मा का स्थानांतरण करते हैं।
● चालन ठोस, द्रव तथा गैस तीनों में संभव होता है।
● ठोस में ऊष्मा स्थानान्तरण केवल चालन विधि द्वारा होता है।
● चालन के दौरान माध्यम का तापमान भी बढ़ जाता है।
ऊष्मा चालकता- किसी भी पदार्थ में चालन विधि द्वारा ऊष्मा संचरित करने का गुण ‘ऊष्मा चालकता’ कहलाती है।
● किसी पदार्थ के लिए ऊष्मा चालकता का मान जितना अधिक होता है। उस पदार्थ में ऊष्मा का आदान-प्रदान उतना ही आसानी से होता है।
● वे पदार्थ जिन मे ऊष्मा का चालन आसानी से होता है, इसके लिए ऊष्मा चालकता गुणांक का मान बहुत अधिक होता है उदाहरण- चाँदी, धातुएँ, अशुद्धि युक्त जल है।
● वे पदार्थ जिनमें ऊष्मा का प्रवाह बहुत कम होता है, ऊष्मा के कुचालक कहलाते हैं। उदाहरण- ऊन, कपड़ा, लकड़ी, काँच, रबर आदि।
● मानव शरीर ऊष्मा का दुर्बल चालक होता है।
● ऊष्मीय चालकता के क्रम-
Kठोस > Kद्रव > Kगैस
Kचाँदी > Kताँबा > Kएल्युमिनियम
Kधातु > Kअधातु
● K = स्थिरांक
● उदाहरण- सर्दियों में ऊनी वस्त्र हमें गर्म रखते हैं क्योंकि उनके रेशों के बीच हवा रहती है, जो ऊष्मा के कुचालक होने के कारण वातावरण की ठंड शरीर तक नहीं पहुँचने देती है।
● जिन घरों में छतें कंक्रीट की बनी होती हैं, वे गर्मियों में अधिक गर्म हो जाती हैं इसका कंक्रीट ऊष्मा का अच्छा चालक होता है।
● चाय को धातु के कप में रखने पर हाथ जल जाता है, लेकिन चीनी-मिट्टी के कप में रखने से हाथ नहीं जलता।
● सर्दियों में लोहे तथा लकड़ी से बनी कुर्सियों को हम हाथ से स्पर्श करते हैं तो लोहा सुचालक होने के कारण हमारे शरीर से ऊष्मा का संचरण आसानी से कर लेता है, जबकि लकड़ी ऊष्मा की कुचालक होने के कारण ऊष्मा का संचरण नहीं हो पाता। अत: लोहे की कुर्सी छूने पर लकड़ी की कुर्सी की अपेक्षा अधिक ठंडी प्रतीत होती है।
● शीत ऋतु में एक मोटा कंबल ओढ़ने की अपेक्षा दो परतों वाले कंबल ओढ़ने पर सर्दी से अधिक सुरक्षा होती है। वायु ऊष्मा की कुचालक होती है, जो कि दो कंबलों की परतों के बीच ऊष्मा-रोधी का कार्य करती है, जिससे ऊष्मा संचरण नहीं हो पाती। इस कारण सर्दी से अधिक सुरक्षा होती है।
● खाना बनाने वाले बर्तनों की पेंदी पर ताँबे की पॉलिश कर दी जाती है, क्योंकि ताँबा ऊष्मा का सुचालक होता है, जो कि पूरे बर्तन पर समान रूप से ऊष्मा को वितरित कर देता है।
2. संवहन- जिसमें पदार्थ के कण एक स्थान से दूसरे स्थान की ओर गति करते हैं, संवहन कहलाती है।
● संवहन द्रव एवं गैसो में होता है।
● गर्म द्रव या गैस हल्के होने के कारण ऊपर की ओर गति करते हैं इस विधि में माध्यम के कण स्वयं गति करते हैं।
● समुद्र की अपेक्षा स्थल अधिक गर्म हो जाता है। क्योंकि जल की विशिष्ट ऊष्मा का मान अधिक होता है।
● समुद्र के अधिक जल आयतन के कारण ऊष्मा वितरित हो जाती है।
● पृथ्वी का वायुमंडल संवहन विधि द्वारा ही गर्म होता है।
● रेफ्रिजरेटर में फ्रीजर ऊपर की ओर बनाया जाता है, क्योंकि फ्रीज के निचले भाग की गर्म वायु ऊपर की ओर उठती है, जो फ्रीजर से टकराकर ठंडी हो जाती है तथा फ्रीजर में उपस्थित ठंडी वायु अधिक घनत्व के कारण नीचे की ओर गति करती है तथा पूरे फ्रीज को ठंडा कर देती है।
3. विकिरण- ऊष्मा स्थानांतरण की ऐसी विधि जिसमें किसी माध्यम की आवश्यकता नहीं होती, विकिरण कहलाती है।
● ऊष्मीय विकिरणों के गुण प्रकाश जैसे ही होते हैं। उदाहरण- सूर्य से पृथ्वी तक ऊष्मा का स्थानान्तरण विकिरण के रूप में होता है।
● इसी कारण से रेगिस्तान दिन में बहुत गर्म तथा रात में अधिक ठंडे हो जाते हैं। क्योंकि ऊष्मा के अच्छे अवशोषक ही अच्छे उत्सर्जक होते हैं।
● साधारण काँच के प्रिज्म से वर्ण विक्षेपण नहीं दर्शाते हैं। इस स्थिति में रॉकसाल्ट या क्वार्ट्ज का प्रयोग किया जाता है।
● सूर्य से पृथ्वी पर ऊष्मा का स्थानांतरण
● गर्मियों के दिनों मे सफेद कपड़े पहनते हैं, क्योंकि सफेद कपड़े ऊष्मीय विकिरण के बुरे अवशोषक होते हैं, वे विकिरण को परावर्तित कर देते हैं, जिससे अधिक गर्मी नहीं लगती।
● यदि जूतों पर पॉलिश करके उनकी सतह चमकदार बना दी गई है तो ऐसे जूते अपने ऊपर पड़ने वाली ऊष्मा को परावर्तित कर देते हैं।
● हमारा शरीर भी वातावरण से ऊष्मा लेता है तथा वातावरण को ऊष्मा देता है यह प्रक्रिया भी विकिरण द्वारा होती है।
महत्वपूर्ण नियम
किरचॉफ का नियम-
इसके अनुसार “अच्छे अवशोषक ही अच्छे उत्सर्जक होते हैं तथा बुरे अवशोषक बुरे उत्सर्जक होते हैं”
● हल्के रंगो की वस्तुओं की अपेक्षा काले रंग की वस्तुएँ विकिरण ऊर्जा का अवशोषण तथा उत्सर्जन अधिक करती है।
● उदाहरण- भैस को गर्मी में ज्यादा गर्मी लगती है एवं सर्दी में ज्यादा ठंड लगती है।
यदि अँधेरे में एक काली एवं सफेद वस्तु को समान ताप पर गर्म करके रख दिया जाये तो किरचॉफ नियम के अनुसार अँधेरे में काली वस्तु अधिक चमेकगी।
स्टीफन का नियम-
इसके अनुसार “किसी वस्तु के एकांक क्षेत्रफल से उत्सर्जित विकिरण ऊर्जा की दर (E) वस्तु के परम ताप (T) के चतुर्थ घात के समानुपाती होती है।“
न्यूटन का शीतलन नियम-
● इसके अनुसार, “किसी वस्तु के ठंडे होने की दर वस्तु के ताप और परिवेश के ताप के बीच अंतर के समानुपाती होती है” शीतलन की दर, वस्तु की सतह के क्षेत्रफल के बढ़ने पर बढ़ती है और घटने पर घटती है।
● यह नियम केवल लघु तापांतर के लिए ही वैध है।
कृष्ण पिंड (Black Body) –
● कोई ऐसी वस्तु जो अपने ऊपर आपतित संपूर्ण विकिरण को अवशोषित कर ले, ‘कृष्ण पिंड’ कहलाती है।
उत्सर्जन क्षमता (Emissive Power) –
● किसी स्रोत के किसी ताप पर उसके प्रति एकांक क्षेत्रफल द्वारा एकांक समय में उत्सर्जित विकिरण को उसकी ‘उत्सर्जन क्षमता’ कहते हैं।
अवशोषण क्षमता (Absorption Power) –
● वस्तु के किसी तल द्वारा अवशोषित ऊष्मा की मात्रा और उसी समय में उस तल पर आपतित कुल ऊष्मा की मात्रा के अनुपात को उस पृष्ठ की ‘अवशोषण क्षमता’ कहते हैं।
पुनर्हिमायन (Regelation) –
● दाब के प्रभाव से बर्फ का निम्न द्रवणांक पर गलना और दाब हटाए जाने पर उसके पुन: जम जाने की क्रिया को ‘पुनर्हिमायन’ कहते हैं।
ओस बिन्दु (Dew Point) –
● वह तापक्रम जिस पर वायुमंडल में मौजूद जलवाष्प ओस में बदल जाए या इसे संतृप्त करने को पर्याप्त हो ‘ओस बिन्दु’ कहलाता है।
ऊष्मा गतिकी (Thermodynomics) –
● यांत्रिकी ऊर्जा और ऊष्मा में संबंध का अध्ययन ऊष्मा गतिकी कहलाती है। ऊष्मा गतिकी भौतिकी की वह शाखा है, जो ऊष्मा तथा ताप की अवधारणा एवं ऊष्मा के अन्य प्रकार की ऊर्जाओं में रूपांतरण का विवेचन करती है।
♦ ऊष्मागतिकी का प्रथम नियम (First Law of Theromdynamics) –
● ऊष्मागतिकी का नियम वास्तव में ऊर्जा संरक्षण के नियम को ही अभिव्यक्ति है। किसी निकाय को दी जाने वाली ऊष्मा दो प्रकार के कार्यों में व्यय होती है।
● निकाय की आतंरिक ऊर्जा में वृद्धि करने में जिससे निकाय का ताप बढ़ता है तथा शेष परिवेश पर कार्य करता है।
● ऊष्मागतिकी का प्रथम नियम-
● Δ�= परिवेश द्वारा निकाय को दी गई ऊष्मा
● Δ� = निकाय द्वारा परिवेश पर किया गया कार्य
● Δ� = निकाय की आतंरिक ऊर्जा में परिवर्तन
♦ ऊष्मागतिकी का द्वितीय नियम (Second Law of Thermodymnamics)
● ऊष्मागतिकी का द्वितीय नियम ऊष्मा के प्रवाहित होने की दिशा को व्यक्त करता है। इस नियम को दो कथनों के रूप में व्यक्त किया जाता है।
● ऐसा कोई प्रक्रम संभव नहीं है, जिसका परिणाम केवल किसी ऊष्मा भंडार से ऊष्मा का अवशोषण करके उसे पूर्णतया कार्य में रूपांतरित करता है। इसे ‘केल्विन प्लैंक’ प्रकथन कहते हैं।
● ऐसा कोई प्रक्रम संभव नहीं है, जिसका परिणाम केवल किसी ऊष्मा का किसी ठंडे पिंड में अपेक्षाकृत गरम पिंड में स्थानांतरण हो।
तापमापी (Thermometer)
वह यंत्र जो किसी वस्तु का ताप मापता है ‘तापमापी’ कहलाता है। पदार्थों के बहुत से भौतिक गुणों में ताप के साथ पर्याप्त परिवर्तन होते हैं।
♦ तापमापी के प्रकार
(1) द्रव तापमापी (Liquid Thermometer)
● सिद्धांत- द्रव तापमापी का सिद्धांत तापमान परिवर्तन के साथ द्रव के आयतन में परिवर्तन पर आधारित होता है। द्रव तापमापी में ऊष्मीय प्रसार (Thermal Expansion) के गुण का प्रयोग होता है।
● द्रव तापमापी में काँच की केशनली में द्रव स्तंभ की लंबाई, ताप मापन के लिए प्रयुक्त होती है।
(i) पारा तापमापी (Mercury Thermomenter)- द्रव तापमापी में पारा का प्रयोग करके पारा तापमापी बनाते हैं। इसका प्रयोग मानव शरीर का ताप मापने में किया जाता है। डॉक्टर के प्रयोग में लेने के कारण इसे ‘क्लीनिकल थर्मामीटर’ भी कहते हैं
● पारा (मर्करी) सामान्यत: त्वरित चाँदी (Quick Silver) के रूप में जाना जाता है। यह एक उत्तम चालक है। अत: यह विद्युत तथा ऊष्मा के प्रवाह में अवरोध पैदा नहीं करता।
(ii) एल्कोहल तापमापी (Alcohal Thermometer)– जब द्रव तापमापी में एल्कोहल का उपयोग करते हैं तो इसे ‘एल्कोहल तापमापी’ कहते हैं। चूँकि एल्कोहल का गलनांक या हिमांक अत्यन्त निम्न जैसे- एथिल एल्कोहल (-1140C) होता है। इसका प्रयोग अति ठंडे प्रदेशों में ताप मापने के लिए करते हैं।
(2) प्लेटिनम प्रतिरोध तापमापी (Platinum Resistance Thermometer)- इस तापमापी द्वारा लगभग 10000C तक का ताप मापा जा सकता है।
● सिद्धांत- इस तापमापी के ताप परिवर्तन के साथ भौतिक गुण प्रतिरोध में परिवर्तन हो उपयोग किया जाता है। किसी धातु के तार का विद्युत प्रतिरोध (Resistance) तार का ताप बढ़ाने पर बढ़ जाते हैं। इस विद्युत प्रतिरोध में हुए परिवर्तन को मापने के सिद्धांत पर यह तापमापी कार्य करता है।
(3) ताप-युग्म तापमापी (Thermocouple Thermo meter) – इस तापमापी द्वारा -2000C 16000C तक का ताप मापा जा सकता है।
● सिद्धांत : जब दो भिन्न-भिन्न धातु युग्मों (ताँबा और लोहा) के तारों को जोड़कर एक बंद परिपथ बनाते हैं ओर दोनों संधियों को भिन्न-भिन्न ताप पर रखते हैं तो परिपथ में विद्युत वाहक बल उत्पन्न हो जाता है और विद्युत धारा प्रवाहित होने लगती है। इसे ‘तापविद्युत धारा’ कहते हैं और इस प्रभाव को सीबेक प्रभाव (Seebeck Effect) कहते हैं।
(4) संपूर्ण विकिरण उच्च तापमापी (Total Radiation Pyrometer)- इसके द्वारा लगभग 8000C से 30000C तक ताप का मापन किया जा सकता है। इसमें ताप वस्तु से उत्सर्जित विकिरण के आधार पर ताप मापते हैं।
● इसका प्रयोग सूर्य के तापमान को मापने में होता है। यह स्टीफन के विकिरण नियम के आधार पर कार्य करता है।
● सिद्धांत-यदि कोई वस्तु उच्च ताप पर है तो वस्तु के प्रति एकांक पृष्ठ क्षेत्रफल से प्रति सेकेंड उत्सर्जित होने वाले विकिरण की मात्रा वस्तु के परम ताप (Absolute Temperature) के चतुर्थ घात के समानुपाती होती है, अर्थात (E�T4) इसे ‘स्टीफन का नियम’ कहते हैं।
(5) स्थिर आयतन गैस तापमापी (Constant Volume Gas Thermometer)-
● हाइड्रोजन गैस तापमापी से लगभग -2000C से 5000C तक का तापमान मापा जा सकता है।
● उच्च ताप पर हाइड्रोजन विसरण के द्वारा बाहर निकलने लगती है अत: 5000C से उच्च तापमान पर (15000C तक) मापन के लिए नाइट्रोजन गैस का उपयोग किया जाता है।
● वहीं -2000C से नीचे (-2680C तक) के ताप मापन हेतु हीलियम गैस का उपयोग होता है।
● सिद्धांत- तापमान में परिवर्तन कराने पर स्थिर आयतन पर हाइड्रोजन गैस के दाब में परिवर्तन हो जाता है। यही गुण इस तापमापी का सिद्धांत है। इस तापमापी में हाइड्रोजन गैस के स्थिर आयतन का दाब मापकर ताप का पता लगाते हैं। इसे प्रमाणिक गैस तापमापी माना जाता है।
(6) प्रकाशित उच्च तापमापी (Optical Pyrometer)
● यह अत्यधिक उच्च तापमान के मापन में प्रयोग किया जाता है। इसके द्वारा लगभग 8000C से 27000C तक ताप मापा जा सकता है।
● सिद्धांत- किसी तप्त वस्तु से उत्सर्जित विकिरण में सर्वाधिक ऊर्जा वाले विकिरण का तरंग दैर्ध्य () तथा वस्तु के परम ताप (T) का गुणनफल नियत रहता है।
=नियतांक इस सिद्धांत को ‘वीन’ (Wien) के विकिरण संबंधी विस्थापन नियम के नाम से जाना जाता है।
अन्य अध्ययन सामग्री
चुम्बक किसे कहते है? प्रकार, गुण, चुंबकीय तरंग, क्षेत्र
ध्वनि किसे कहते हैं? परिभाषा, गुण, लक्षण, प्रकार ( Dhwani kya hai )
गुरुत्वाकर्षण बल किसे कहते हैं? परिभाषा, सूत्र, नियम, Gravitational force in hindi
महत्वपूर्ण प्रश्न
ऊष्मा क्या है परिभाषा दीजिए?
किसी पदार्थ के गर्म या ठंडे होने के कारण उसमें जो ऊर्जा होती है उसे उसकी ऊष्मीय ऊर्जा कहते हैं।
ऊष्मा इकाई कौन सी है?
ऊष्मा की SI इकाई जूल है।
ऊष्मा का सूत्र क्या होता है?
गुप्त ऊष्मा का सूत्र L = Q/M